Hors-AMM : Accès dérogatoires & autres usages
Les usages hors-AMM correspond à toute utilisation d’un médicament en dehors de son autorisation. Tous les accès dérogatoires sont du hors-AMM, mais tout le hors-AMM n’est pas un accès dérogatoire.
En France, les patients en impasse thérapeutique, notamment atteints de maladies graves ou rares, peuvent accéder à des médicaments non autorisés pour leur indication. La réforme de 2021 a instauré trois dispositifs : les autorisations d’accès compassionnel (AAC), les autorisations d’accès précoce (AAP) et les cadres de prescription compassionnelle (CPC). Ces mécanismes, encadrés notamment avec la HAS, facilitent l’accès à des traitements innovants, en particulier pour les patients pédiatriques.
La prescription hors-AMM individuelle
- Utilisation d’un médicament en dehors des indications validées officiellement ou selon des modalités différentes (dose, population, voie d’administration…)
- AMM délivrée en Europe par des autorités comme l’Agence européenne des médicaments (EMA) ou en France par l’Agence nationale de sécurité du médicament et des produits de santé (ANSM)
Modalités de prescription
- Par le médecin, s’il n’existe pas d’alternative appropriée ou s’il existe des données scientifiques suffisantes et si c’est dans l’intérêt du patient
- Le médecin engage sa responsabilité et doit informer le patient, justifier sa décision (données scientifiques, recommandations), assurer un suivi renforcé et mentionner « hors-AMM » sur l’ordonnance
Différents cadres possibles
Hors-AMM « simple »
- Décision individuelle du médecin basée sur la littérature/recommandations, très fréquente en pratique (ex. : pédiatrie, oncologie, …)
Hors-AMM encadré
- Protocole interne ou institutionnel : suivi organisé des patients par collecte de données permettant une sécurisation de la pratique
- Accompagné d’un protocole d’utilisation thérapeutique avec suivi des patients (PUT-SP)
Modalités de prise en charge
Consulter le document d’aide à la prescription
- Obtenir un accord en RCP du centre de référence, informer le patient des risques et de l'absence d'alternative
- Déposer un dossier auprès du service médical de l'Assurance Maladie (avec CR de RCP, historique médical, bibliographie et PNDS)
- Prescription doit explicitement mentionner le caractère hors AMM et l'accord de prise en charge obtenu
- Prise en charge dérogatoire par l'Assurance Maladie possible si la spécialité figure dans une recommandation HAS/ANSM
Les accès dérogatoires
Formes spécifiques et encadrées de hors-AMM et supervisées notamment par l’ANSM et la HAS
- Référentiels des spécialités en accès dérogatoires en France
Autorisation d’Accès Précoce (AAP)
- Les accès précoces (AAP) – ANSM
- Référentiel des AAP
AAP pré-AMM
- Pour un médicament n’ayant pas encore d’AMM dans l’indication concernée et destiné à être commercialisé (présumé innovant, avec données cliniques disponibles ou en cours de recueil)
- Demande : à l’initiative du laboratoire et via la plateforme Sésame (HAS)
- Evaluation : par la HAS après avis de l’ANSM (uniquement médicaments pour lesquels aucun avis du CHMP* n’a encore été émis, LFSS pour 2023) sur le critère d’évaluation de la balance bénéfice-risque
- Durée de validité : 1 an renouvelable
*Committee for Medicinal Products for Human Use (dépendant de l’EMA)
L’AAP est subordonnée au respect d’un protocole d’utilisation thérapeutique et de recueil des données (PUT-RD) apportant aux prescripteurs/patients toute informations pertinentes sur le médicament/utilisation :
- Description du médicament, des conditions d’utilisation et de prescription complétés par le RCP
- Documents d’information que le prescripteur doit remettre au patient avant toute prescription du médicament sur : l'accès précoce à un médicament avant l'AMM, l'accès précoce à un médicament après l'AMM, le traitement des données personnelles
- Organise la surveillance des patients (recueil des effets indésirables et situations particulières)
- Recueil de données relatives à l’utilisation du médicament
Accès précoce à un médicament avant AMM
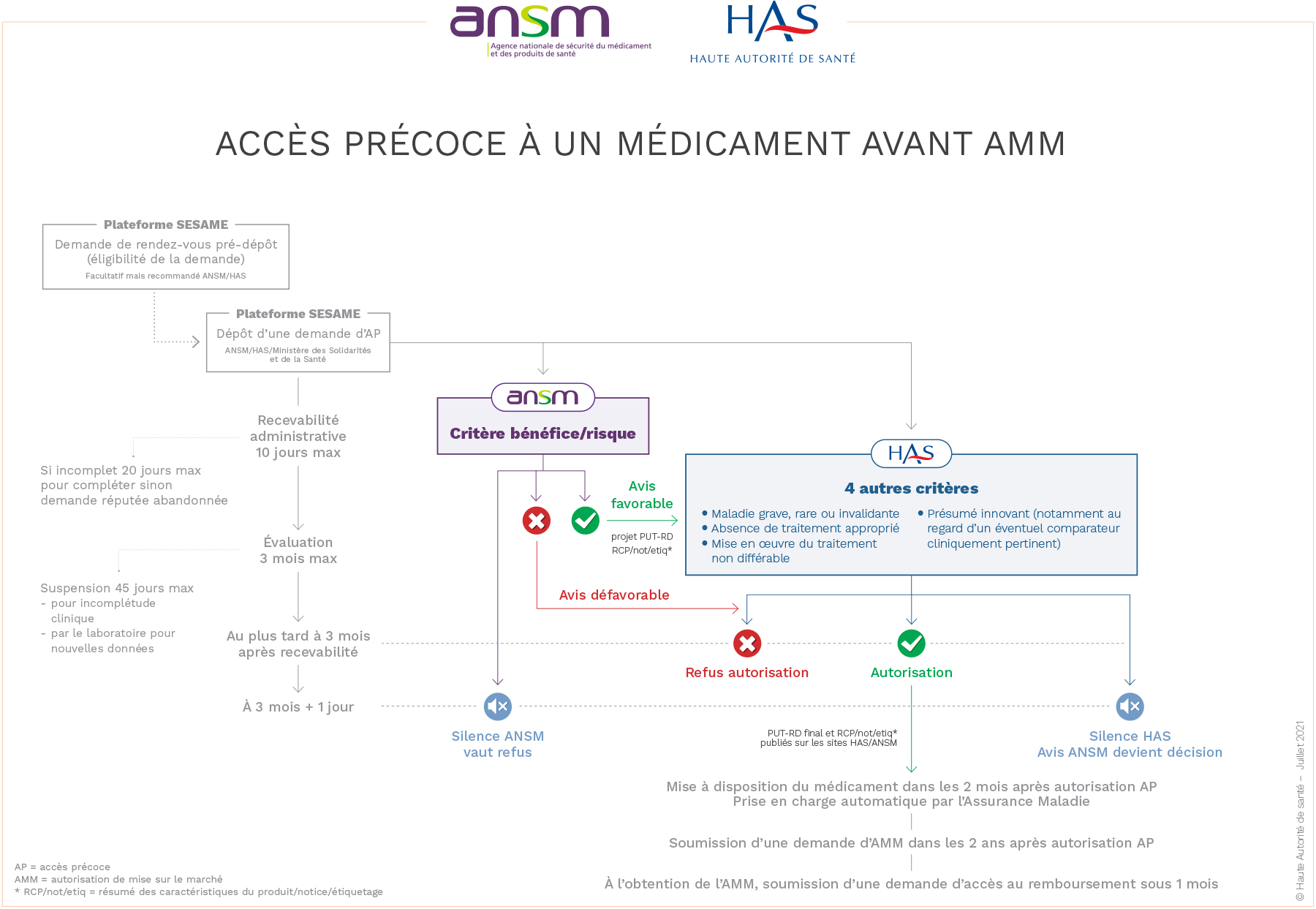
Source : https://ansm.sante.fr/documents/reference/medicaments-en-acces-derogatoires/les-acces-precoces-aap
AAP post-AMM
- Pour un médicament ayant obtenu son AMM mais qui n’est pas encore remboursé, ni disponible en routine (prix et remboursement en attente de négociation
- Maintien d’un accès anticipé pour les patients pendant cette période : évite un non accès au traitement entre l’obtention de l’AMM et la décision de remboursement par les autorités
Accès précoce à un médicament après AMM
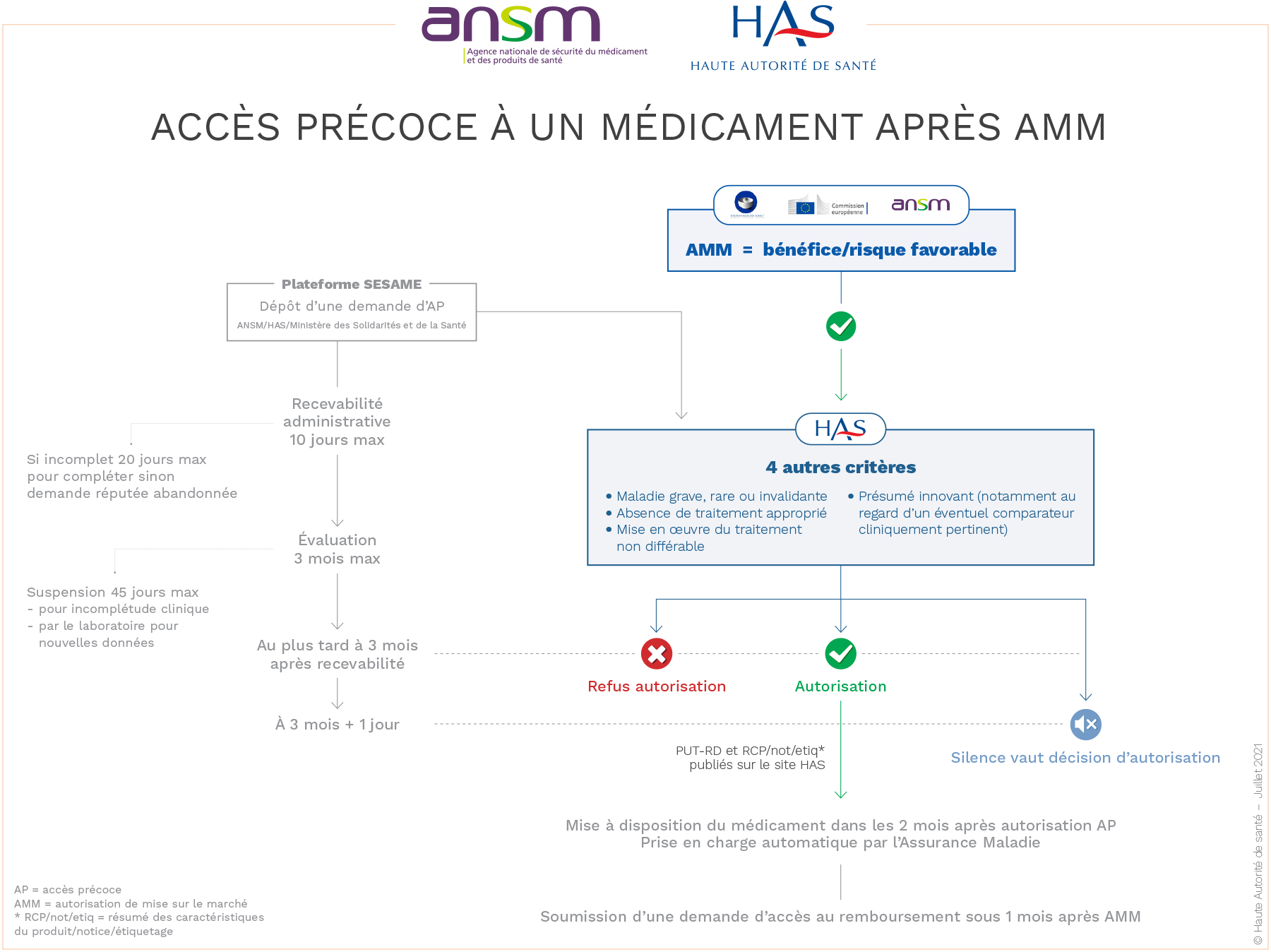
Source : https://ansm.sante.fr/documents/reference/medicaments-en-acces-derogatoires/les-acces-precoces-aap
L’accès précoce dans le parcours du médicament
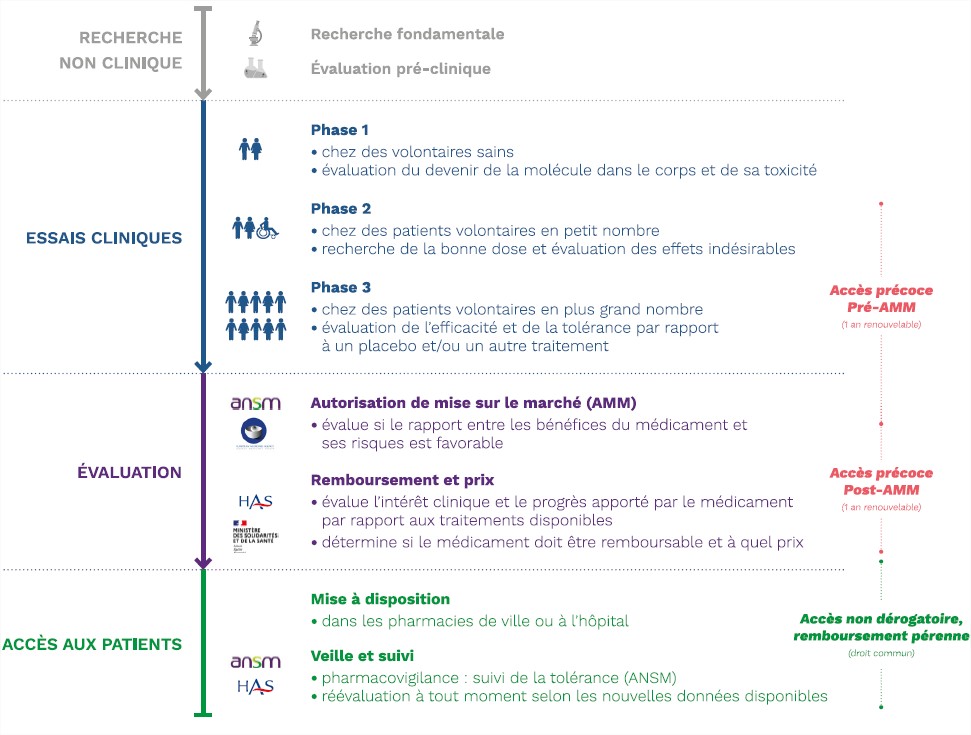
Source : https://www.has-sante.fr/jcms/p_3274374/fr/medicament-en-acces-precoce-ce-qu-il-faut-savoir
Prescription pour l’AAP
Rôles du prescripteur :
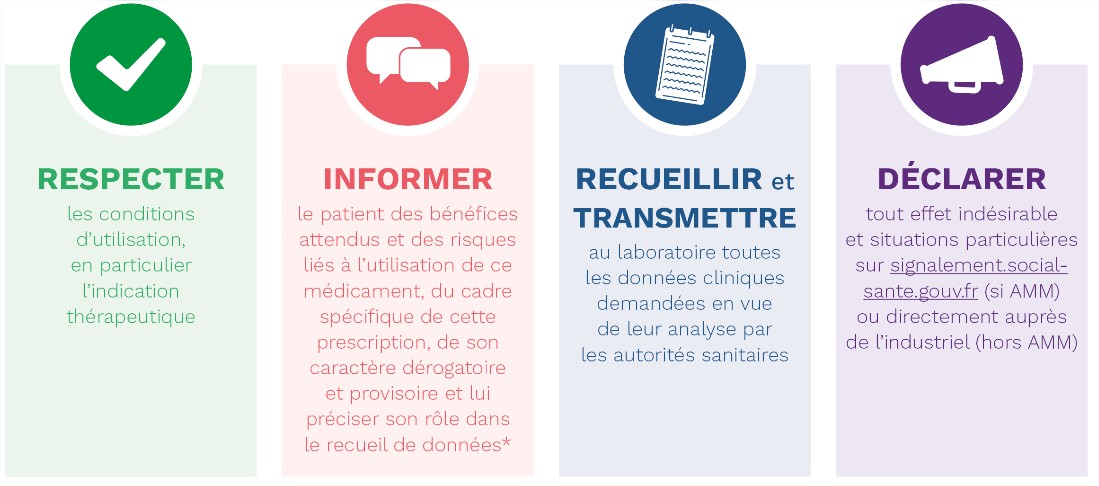
Prescrire un médicament en accès précoce
Avant toute prescription : le prescripteur doit remettre au patient une fiche d’information
Pour un adulte
- Accès précoce avant autorisation de mise sur le marché
- Accès précoce après autorisation de mise sur le marché
- Traitement des données à caractère personnel
Pour un enfant
- Accès précoce avant autorisation de mise sur le marché
- Accès précoce après autorisation de mise sur le marché
- Traitement des données à caractère personnel
Prise en charge de l’AAP
Établissement de santé :
- Le laboratoire doit garantir la continuité des traitements initiés pendant 1 an après l’arrêt de cette prise en charge :
- 3 mois pris en charge par l’Assurance Maladie
- 9 mois où le laboratoire peut choisir de fournir le traitement gratuitement
- Informations sur la continuité des traitements : centralisées dans le référentiel du ministère
- Spécialités inscrites sur la liste des médicaments remboursables aux assurés sociaux : entrée en vigueur des arrêtés (inscription, prix, taux de participation) différée de 15 jours après la publication au Journal Officiel
- Arrêt de prise en charge coïncidera avec l’application des arrêtés
Patient : prise en charge du médicament sans reste à charge
Industriel : indemnité tarifaire librement fixée par celui-ci (à l’exclusion des cas où le médicament bénéficie déjà d’un prix administré) et mécanisme de remises annuelles (reversement d’une partie de son chiffre d’affaires à l’Assurance Maladie, sous forme de remises annuelles a posteriori)
Autorisation d’Accès Compassionnel (AAC)
AAC classique
- Permet un accès au médicament qui ne possède pas d’AMM en France
- Demande : à l’initiative du prescripteur via la plateforme e-Saturne (ANSM) pour un patient donné et pour un médicament n’ayant pas vocation à être commercialisé en France par le laboratoire
- Durée de validité : 1 an renouvelable
AAC pré-précoce (cas particulier d’AAC)
- Situation transitoire entre le système compassionnel et précoce
- Par dérogation, il est prévu que l’ANSM puisse octroyer une AAC sur demande d’un médecin prescripteur, pour des médicaments qui font l’objet de recherche clinique dans une indication considérée à un stade très précoce
Dérogation pour les médicaments :
- faisant l’objet de recherche clinique (indication considérée à un stade très précoce
- tendant vers une volonté d’obtenir une AMM (essais cliniques en cours)
- dont l’entreprise titulaire des droits d’exploitation s’engage à déposer une demande d’accès précoce dans un délai déterminé par décret (12 mois si cas général, 18 mois si maladie rare et prorogations possibles par 6 mois en fonction du contexte)
Conditions à respecter : maladies graves, rares ou invalidantes, dont la mise en œuvre ne peut être différée
Schéma de l’évolution attendue d’un médicament en AAC pré-précoce

Source : https://www.omedit-idf.fr/thematiques/ap_ac/
Prescription pour l’AAC
- Prérequis : doit être précédée par une information orale et écrite de chaque patient par le prescripteur sur le caractère compassionnel et dérogatoire de la prise en charge du médicament
- Demande : via la plateforme e-Saturne (ANSM) et transmise par le pharmacien de la PUI (via e-Saturne)
- Autorisation (ou non) : par l’ANSM et pour la durée de traitement du patient considéré (limite maximale d’un an)
- Dispensation : par la Pharmacie à Usage Intérieur (PUI) de l’hôpital
- Disponibilité du médicament : administration hospitalière ou rétrocession par les PUI si le médicament ne relève pas de la réserve hospitalière
Prise en charge de l’AAC
Etablissement de santé :
- Référentiel « liste en sus »avec codes UCD (Unité Commune de Dispensation) et codes indications concernés par cette prise en charge
- Financement en sus des GHS (Groupe Homogènes de Séjours - tarif forfaitaire versé à un établissement pour un séjour donnée basé sur le GHM/type de prise en charge) au fil de l’eau
- Rétrocession : médicament pris en charge à 100 % dès l’autorisation. Le prix facturé inclut TVA (2,1 %) et marge forfaitaire. Transmission du code indication via le RSF-ACE (Résumé Standardisé de Facturation – Actes et Consultations Externes) pour les traitements relevant de l’AAC ou d’une continuité de traitement, afin d’assurer leur prise en charge.
Patient : prise en charge du médicament sans reste à charge
Industriel : indemnité tarifaire librement fixée par l’industriel (à l’exclusion des cas où le médicament bénéficie déjà d’un prix administré) et mécanisme de remises annuelles (l’industriel reverse une partie de son chiffre d’affaires à l’Assurance Maladie, sous forme de remises annuelles a posteriori)
Officine : ne pourra concerner que les médicaments faisant l’objet d’un CPC et la dispensation en ville sera définie par dérogation et accordée par arrêté
Cadre de Prescription Compassionnelle (CPC)
- Encadre l’utilisation d’un médicament en dehors de son AMM et peut concerner un médicament qui n’a pas vocation à être commercialisé dans l’indication visée
- Objectif : sécuriser la prescription d’un médicament utilisé en hors-AMM, afin de répondre à des besoins spécifiques de certains patients (décret n°2022-164 du 11 février 2022)
- Instauration : à la suite d’un signalement provenant de l’Institut National du Cancer (INCa), des conseils nationaux professionnels, des Filières de Santé Maladies Rares (FSMR), des associations de patients
- Evaluation et suivi : par l’ANSM
Prescription du CPC
- Doit être précédée par une information orale et écrite de chaque patient par le prescripteur sur le caractère compassionnel et dérogatoire de la prise en charge du médicament
Les AAC/AAP/CPC en pratique
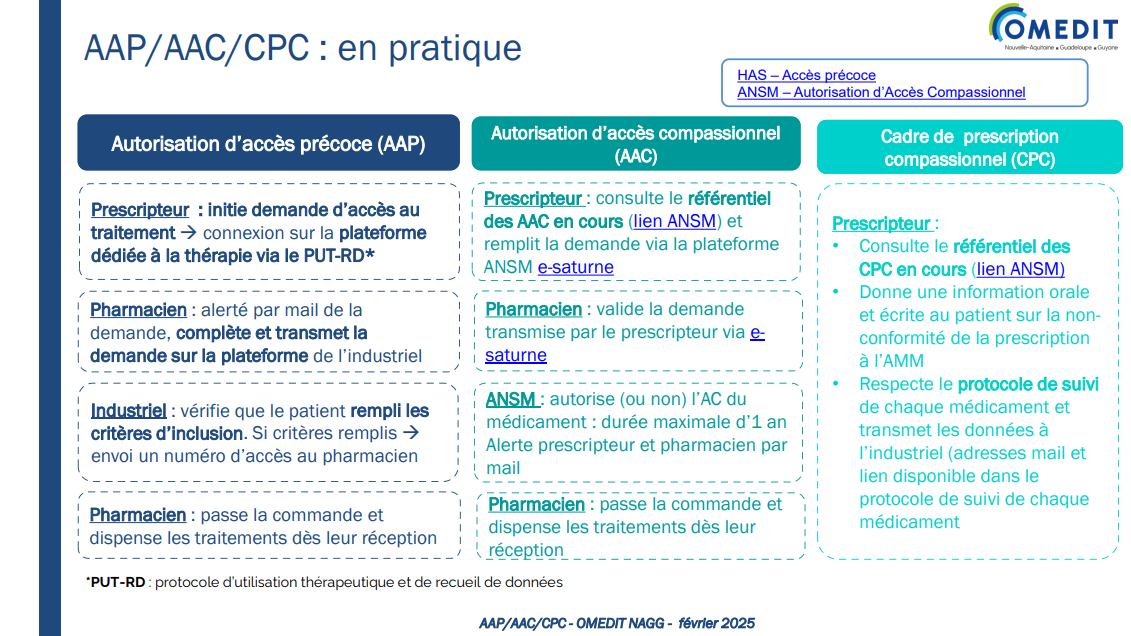
Source : https://www.omedit-nag.fr/medicaments-en-acces-precoce-acces-compassionnel
Spécialités en accès dérogatoires utilisées à la filière OSCAR
Vorasidenib (VORANIGO®)
Laboratoires SERVIER, 10 mg et 40 mg, comprimé pelliculé
AAP : en monothérapie pour le traitement de l'astrocytome ou de l'oligodendrogliome de grade 2 chez les patients adultes et adolescents âgés de 12 ans et plus
Liste des spécialités en accès dérogatoire - Vorasidenib - ANSM
Ivosidenib (TIBSOVO®)
Laboratoires SERVIER, 250 mg en comprimé
CPC :traitement en monothérapie des patients adultes atteints d’un gliome de bas grade IDH1 muté, inopérables, non répondeur ou en progression après : un traitement par radiothérapie ou y étant inéligible et au moins une ligne de chimiothérapie à base de témozolomide ou y étant non éligible
Liste des spécialités en accès dérogatoire - Ivosidenib - ANSM
BMN (anciennement INZ-701)
Laboratoires Biomarin, 10 mg et 25 mg en poudre pour solution injectable
AAC : GACI de type 2, confirmé génétiquement et compatible avec une déficience fonctionnelle d’ABCC6 chez des patients âgés de moins de 12 mois au moment du diagnostic
Liste des spécialités en accès dérogatoire - INZ-701 - ANSM
Palopegtériparatide (YORVIPATH®) – TransCon PTH
Laboratoires Ascendis, 168 µg/0,56 mL, 294 µg/0,98 mL et 420 µg/1,4 mL en stylo prérempli pour injection sous-cutanée
AAP : traitement des adultes atteints d’hypoparathyroïdie chronique pour lesquels une thérapie substitutive en PTH est nécessaire et qui ne sont pas contrôlés de manière optimale par le traitement vitamino-calcique
https://www.has-sante.fr/jcms/p_3545107/fr/yorvipath-palopegteriparatide-hypoparathyroidie-chronique
Palovarotène (SOHONOS®)
Laboratoires Ipsen, 1 mg, 1,5 mg, 2,5 mg, 5 mg et 10 mg en capsule orale
AAC : Fibrodysplasie ossifiante progressive pour les sujets avec un squelette radiologiquement mature
https://ansm.sante.fr/tableau-acces-derogatoire/sohonos#
Anakinra (KINERET®)
Laboratoires Swedish Orphan Biovitrum,100 mg/jour en seringue préremplie pour injection sous-cutanée
AAC : Calcinose tumorale familiale (CTF)
Asfotase alfa (STRENSIQ®)
Laboratoires Alexion, 40 mg/mL et 100 mg/mL en solution injectable
AAC : Hypophosphatasie infantile (HPP)
Trofinetide (DAYBUE®)
Laboratoires Acadia, 200/mL en solution buvable
AAC : Syndrome de Rett
Dérogation pour dispositif médical (DM) dépourvu de marquage CE
Dérogation individuelle
- Le professionnel de santé transmet à l’opérateur de marché (surveille l'évolution des cours et des tendances du marché) les éléments justifiant l’intérêt pour la santé publique ou pour le patient (et toute information utile, données cliniques) afin que celui-ci puisse constituer une demande de dérogation individuelle auprès de l’ANSM
- Analyse de la demande : par l’ANSM qui adresse une réponse motivée à l’opérateur et au professionnel de santé
Si accord
- L’opérateur est autorisé à fournir le dispositif concerné à l’établissement de santé.
- Le professionnel de santé devra :
- Informer le patient de manière claire et préalable à l’utilisation du dispositif et recueillir son consentement
- Signaler tout incident ou risque d’incident lié à l’utilisation du dispositif médical
Si refus
- L’opérateur ne peut pas fournir le dispositif à l’établissement de santé
Dérogation globale
- Le professionnel de santé commande auprès de l’opérateur un dispositif dépourvu de marquage CE et figurant sur la liste des dérogations globales accordées en motivant sa demande
- Le professionnel de santé doit :
- Informer clairement le patient en amont qu’il s’agit d’un dispositif sans marquage CE
- Recueillir son consentement
- Déclarer tout incident ou risque d’incident lié à l’utilisation du dispositif médical
